Malattia di Alzheimer: sintomi, stadi, possibilità di cura
La malattia di Alzheimer o morbo di di Alzheimer è una malattia neurodegenerativa caratterizzata da un deterioramento cognitivo cronico progressivo ed è la prima causa di demenza nel mondo.
La demenza è un’alterazione globale, spesso irreversibile e progressiva delle funzioni cerebrali corticali e colpisce tutte le funzioni cognitive, sensoriali e motorie. In particolare, sono alterate le abilità percettivo-motorie, le abilità sociali e il controllo delle reazioni emotive con comportamenti disforici. Il progressivo deterioramento delle funzioni cerebrali conduce l’individuo alla perdita dell’autonomia nelle attività della vita quotidiana e nella cura del sé e si verifica un progressivo ottundimento della coscienza fino allo stato vegetale.
Classificazione Eziopatogenetica – Forme di Alzheimer
E’ possibile distinguere, sulla base del meccanismo eziopatogenetico, due forme di Alzheimer:
- Alzheimer Sporadico: costituisce il 75-90% dei casi, è una malattia a insorgenza tardiva, manifestandosi oltre i 65 anni di età, ed è una malattia con causa multifattoriale (le cause geniche più frequenti sono a carico di APP e delle preseniline 1 e 2)
- Alzheimer Familiare o Ereditario: costituisce il 10-25% dei casi, è una malattia a insorgenza precoce, manifestandosi sotto i 65 anni di età, ed è una malattia autosomica dominante (la causa genica più frequente è a carico di APO E)

Epidemiologia della malattia di Alzheimer
Secondo il World Alzheimer Report del 2015 (un autorevole rapporto che include una rassegna critica dei dati relativi a tendenze e previsioni su prevalenza, incidenza e costi della demenza a livello mondiale), ci sono (dati aggiornati al 2015) nel mondo 46,8 milioni di persone affette da una forma di demenza. Tale cifra è destinata quasi a raddoppiare ogni 20 anni, raggiungendo 74,7 milioni di persone nel 2030 e 131,5 milioni nel 2050. Queste stime risultano del 12-13% più alte rispetto alle stime pubblicate nel World Alzheimer Report del 2009. Ogni anno si stimano, su scala mondiale, circa 9,9 milioni di nuovi casi all’anno di demenza, ovvero un nuovo caso ogni 3 secondi circa.
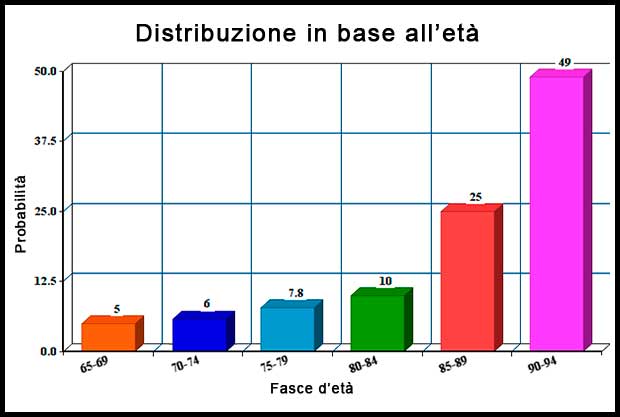
Il principale fattore di rischio per Alzheimer è l’età. L’incidenza della demenza aumenta esponenzialmente con l’avanzare dell’età. Passa da 3,9 casi all’anno ogni 1.000 persone con età compresa tra i 60 e i 64 anni, a 104,8 casi all’anno ogni 1.000 persone di età maggiore a 90 anni. La distribuzione geografica dei nuovi casi di demenza mostra che il 49% del totale interessa l’Asia, il 25% l’Europa, il 18% le Americhe e l’8% l’Africa. Il 58% di tutte le persone con demenza vive in Paesi classificati dalla Banca Mondiale come a reddito medio o basso. Si stima che tale percentuale sia destinata ad aumentare, raggiungendo il 63% nel 2030 e il 68% nel 2050. Esiste una netta prevalenza di malattia nel sesso femminile, che appare indipendente dalla loro maggiore vita media: si ipotizza che la carenza di estrogeni che si instaura durante il periodo post-menopausale sia un fattore di rischio.
La malattia di Alzheimer costituisce un enorme costo socio-sanitario: i costi globali della demenza, che includono i costi diretti e indiretti relativi alle cure mediche e assistenziali, sono cresciuti da 604 miliardi di dollari nel 2010 a 818 miliardi di dollari nel 2015, registrando un aumento del 35,4%. Quasi tutte le proiezioni riguardanti l’incombente epidemia di demenza presuppongono che le tendenze attuali restino invariate nel tempo e che l’unico fattore determinante gli aumenti stimati sia l’invecchiamento della popolazione.
Fattori di rischio per malattia di Alzheimer
FATTORI GENETICI
E’ stata dimostrata la correlazione tra la presenza di specifiche mutazioni genetiche e sviluppo di malattia di Alzheimer. I principali geni attualmente conosciuti come coinvolti nella patogenesi della malattia sono:
- gene della proteina amiloide (APP) localizzato sul Cr21 – AD1 (Malattia di Alzheimer tipo 1): mutazioni rare (20 famiglie nel mondo); esordio precoce (35-50 aa);
- gene della apolipoproteina E (APOE) localizzato sul Cr19 – AD2: associato anche a forme sporadiche esordio tardivo (>65 aa); l’apolipoproteina E è presente nel tessuto nervoso, prodotta dalle cellule gliali, ed è coinvolta nella clearance della B-proteina: una sua alterazione ne compromette l’efficienza;
- gene della presenilina 1 (PSEN1) localizzato sul Cr14 – AD3: > 50 mutazioni identificate; causa genetica più comune di AD familiare ad esordio precoce (28-60 aa); forma più grave in assoluto;
- gene della presenilina 2 (PSEN2) localizzato sul Cr1 – AD4: esordio meno precoce, andamento meno grave rispetto a PSEN1. Le preseniline 1 e 2 sono due proteine omologhe implicate nei meccanismi di maturazione e trasporto intracellulare della proteina APP.
Si pensa, tuttavia, che una larga quota di forme familiari sia causata da alterazioni genetiche ancora ignote.
FATTORI DI RISCHIO VASCOLARI
- Ipertensione sistolica (>160 mmHg);
- colesterolo sierico > 6.5 mmol/L.
FATTORI DI RISCHIO DOVUTI ALLO STILE DI VITA
- Fumo di tabacco;
- scarsa attività fisica;
- eccessivo consumo di alcool;
- traumatismi cranici.
FATTORI DI RISCHIO SOCIO-DEMOGRAFICI
- Età avanzata: il rischio aumenta all’aumentare dell’età;
- sesso femminile;
- periodo di istruzione < 15 anni;
- lavoro che espone a tossine ambientali (es. metalli pesanti).
ALTRI FATTORI:
- Infezioni virali;
- depressione;
- PAN (anamnestica);
- ipertiroidismo;
- familiarità per s. di Down.
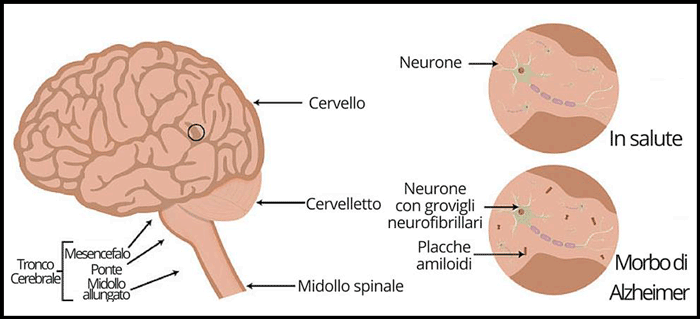
Eziopatogenesi
Le lesioni istologiche caratteristiche dell’Alzheimer sono le placche amilodi, i grovigli neurofibrillari e la presenza di rarefazione neuronale.
Le placche “amiloidi” o neuritiche (extra-neuronali) si trovano solo a livello del sistema nervoso centrale. Si tratta di strutture di forma sferoidale, costituite da un deposito centrale di amiloide, circondato da materiale granulare e filamentoso rappresentato da neuriti rigonfi ed espansioni dendritiche frammiste a processi gliali e cellule microgliali. La composizione e la configurazione delle placche senili variano a seconda del loro stadio di sviluppo. La sostanza amiloide, componente essenziale delle placche senili, è principalmente composta da una proteina, la Beta-proteina, che è un peptide di 40-42 aminoacidi che deriva dalla proteolisi di un precursore di maggiori dimensioni, la proteina APP (Amyloid Protein Precursor), particolarmente espressa nei neuroni e il cui gene si trova sul cromosoma 21. La beta-proteina ha la proprietà, insita nelle sue caratteristiche fisico-chimiche di formare spontaneamente degli aggregati di fibre amiloide in modo proporzionale alla loro concentrazione.
La Beta-proteina è prodotta per l’azione di due proteasi intracellulari, chiamate Beta e gamma secretasi, sul precursore APP: questi due enzimi portano alla formazione di due distinti frammenti di beta-proteina, uno composto da 40 aminoacidi e uno composto da 42 aminoacidi. Essi si trovano normalmente a basse concentrazione nei fluidi extracellulari, nel plasma e nel liquor. Di contro, nel cervello di soggetti sani la B-proteina è completamente assente grazie a meccanismi, ancora non completamente chiariti, che provvedono alla sua eliminazione.
Nella malattia di Alzheimer l’aumentata produzione o la ridotta eliminazione di Beta-proteina da 42 aminoacidi ne causa l’accumulo fino al raggiungimento di una concentrazione critica che ne provoca la polimerizzazione. Questo innescherebbe dei meccanismi di stress ossidativo, alterazioni del citoscheletro e fenomeni degenerativi che culminerebbero nella morte neuronale.
Il ruolo dell’accumulo di Beta-proteina nella patogenesi dell’Alzheimer è sostenuto dal fatto che malattie genetiche che determinano un’aumentata produzione di Beta-proteina sono invariabilmente connesse con un quadro di Alzheimer: nella sindrome di Down, ad esempio, la presenza di una triplice copia del cromosoma 21 provoca un’aumentata produzione di APP e dunque di Beta-proteina con sviluppo precoce di alterazioni cerebrali caratteristiche dell’Alzheimer.
Nei casi sporadici di malattia (dove cioè non è riscontrabile la presenza di una specifica mutazione genetica o una causa che giustifichi l’aumento della concentrazione di beta-proteina) l’ipotesi del danno neuronale prevede che fattori legati all’invecchiamento modifichino il metabolismo dell’APP favorendo la produzione di beta-proteina, con degenerazione e morte neuronale. A sua volta, la morte neuronale induce l’accumulo dell’APP, per cui si crea un circolo vizioso autoalimentato. Questo spiega l’esistenza di una sinergia tra fattori di rischio per demenza vascolare (diabete, ipertensione, malattia coronarica, ipercolesterolemia ecc.) nell’insorgenza della malattia di Alzheimer.
I grovigli neurofibrillari o neurofibrillary tangles (intra-neuronali) sono masse di filamenti abnormi di forma globosa o “a fiamma” situate a livello del citoplasma perinucleare e che spesso si estendono sino ai dendriti apicali;. Al microscopio ottico presentano una struttura fibrillare e sono costituiti da polimeri di proteina tau, che è una proteina che ha la funzione fisiologica di promuovere la polimerizzazione della tubulina in microtubuli. Nei filamenti patologici la proteina tau appare iperfosforilata e ciò impedisce la normale formazione dei microtubuli.
Nella corteccia cerebrale dei pazienti affetti da malattia di Alzheimer si osserva la presenza di rarefazione neuronale: in particolare a carico dei neuroni del terzo e quinto strato del lobo frontale e temporale. Può essere molto marcata la perdita neuronale in alcuni nuclei sottocorticali quali il nucleo basale, il nucleo dorsale del rafe e il locus coerules con riduzione del contenuto di neurotrasmettitori cerebrali. Coinvolto tipicamente anche l’ippocampo, fondamentale nella conservazione della memoria.
L’ipotesi dopaminergica
Secondo una recente ipotesi, proposta da un gruppo di ricercatori della Fondazione Santa Lucia Irccs, dell’Università Campus Bio-Medico di Roma e del CNR, nella patogenesi dell’Alzheimer sarebbe coinvolta un’area cerebrale molto meno studiata fino ad ora, l’area tegmentale ventrale, i cui neuroni rilasciano dopamina agendo su diverse aree del cervello, tra cui l’ippocampo. E’ stato visto che in modelli animali, affetti da forme genetiche di malattia di Alzheimer, si verifica una degenerazione precoce a livello dei neuroni della sostanza tegmentale ventrale con conseguente riduzione delle efferenze dopaminergiche; inoltre, alla somministrazione di L-dopa (precursore della dopamina utilizzata nel trattamento della malattia di Parkinson) si è ottenuto un miglioramento della memoria.
Per approfondimento consultare il seguente articolo, pubblicato su Nature Communications: “Dopamine neuronal loss contributes to memory and reward dysfunction in a model of Alzheimer’s disease”
Alzheimer – Sintomi
Schematicamente è possibile distinguere diverse fasi di malattia anche se la malattia è caratterizzata da un’ampia variabilità nella comparsa dei sintomi.

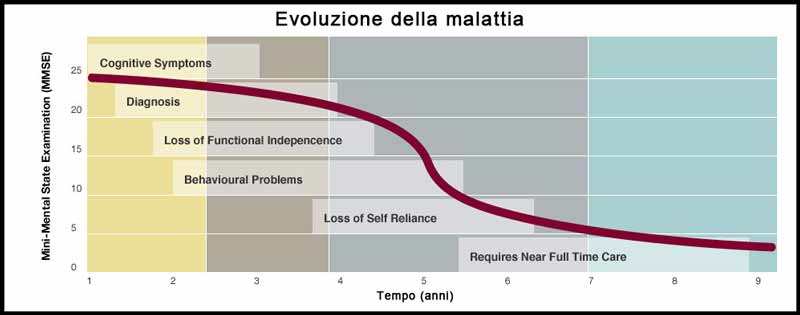
Fasi della malattia di Alzheimer
- Fase iniziale: l’esordio della malattia è spesso caratterizzato dalla perdita progressiva della memoria recente, all’inizio circoscritta a sporadici episodi nella vita quotidiana (il soggetto non ricorda cosa ha mangiato a pranzo o di presentarsi a un appuntamento); in seguito compaiono deficit di attenzione con difficoltà nel mantenere adeguati rapporti interpersonali, calo delle capacità verbali, calo dell’iniziativa e degli interessi. In genere il paziente è consapevole delle proprie difficoltà cognitive e questo determina una reazione depressiva.
- Fase intermedia: in questa fase il deficit della memoria è molto evidente, con difficoltà nel ricordare le informazioni apprese di recente, disturbi attentivi e problemi nel pianificare azioni, di giudizio e di critica. Si accentua il disturbo del linguaggio con comparsa di anomie (incapacità a denominare oggetti o persone). Il rendimento lavorativo e la partecipazione alla vita sociale sono ridotti. Insorgono anche disturbi del linguaggio, sia parlato che scritto.
- Fase finale: quali sono i sintomi finali dell’Alzheimer? Il disturbo della memoria si estende a coinvolgere anche la componente retrograda (a lungo termine), la memoria semantica (le conoscenze apprese) e la memoria procedurale (le informazioni riguardo l’ordine di azioni per eseguire una certa procedura). Il soggetto diventa apatico, ritirato, indifferente alle sollecitazioni esterne e noncurante della propria condizione. E’ incapace di curare i propri bisogni personali fino alla totale dipendenza nelle attività della vita quotidiana (ADL). Spesso non riconosce più gli oggetti e le persone, anche i familiari più stretti, ed è disorientato nel tempo e nello spazio. Compaiono alterazioni comportamentali: ansia, depressione, confusione e, talvolta, deliri e allucinazioni.
- Fase terminale: la morte sopravviene, il più delle volte, a causa di complicanze mediche conseguenti la malattia, soprattutto infezioni.
Molto spesso la malattia di Alzheimer, soprattutto nelle fasi iniziali, è mal diagnosticata: è frequente una errata diagnosi di demenza di diverso tipo, depressione, normale invecchiamento, esiti di ictus concomitante, nessuna diagnosi, altro.
Alzheimer Precoce o Giovanile
Raramente (10-15% dei casi) la malattia di Alzheimer insorge al di sotto dei 60 anni di età: si tratta dell’Alzheimer precoce o Alzheimer giovanile. Esso ha una base ereditaria, genetica. La diagnosi di questi casi è difficile perché i sintomi cognitivi possono essere diversi rispetto alla classica forma a esordio più tardivo. I sintomi iniziali possono non interessare la memoria bensì comprendere disturbi comportamentali, del linguaggio o delle funzioni esecutive.
Prognosi
Quanto vive un malato di Alzheimer? Posto che il decorso della malattia ha un’ampia variabilità inter-individuale, che può essere influenzato dalla compresenza di altre patologie, l’aspettativa di vita media a partire dalla diagnosi di malattia è di 6-8 anni. Soltanto il 3% sopravvive per oltre 15 anni.
Diagnosi di Malattia di Alzheimer
La diagnosi di AD può essere posta con ragionevole certezza usando precisi criteri diagnostici clinici. Nel 1984 l’associazione dei malati di Alzheimer e la statunitense National Neurological Disorders and Stroke (NINCDS) hanno istituito il criterio diagnostico NINCDS-ADRDA, successivamente aggiornato nel 2007, che avrebbe un’accuratezza (verificata dall’autopsia) di circa il 90%.
Diagnosi di Alzheimer possibile: quando è presente una sindrome demenziale, senza disturbi di coscienza, e sono state escluse altre cause neurologiche, psichiatriche o sistemiche che possano spiegare i sintomi.
Diagnosi di Alzheimer probabile: quando è presente una sindrome demenziale sulla base della clinica e dei risultati di test quali il Mini Mental State e la scala di Blessed. Devono essere esclude sulla base della clinica o di esami diagnostici complementari, la presenza di altre patologie che possano giustificare i disturbi del paziente.
Diagnosi di Alzheimer certa o definita: si ottiene unicamente sulla base della diagnosi istopatologica, ovvero dall’analisi del materiale autoptico.
Esami complementari:
L’esame del liquido cefalorachidiano e gli esami biumorali non sono dirimenti.
L’elettroencefalogramma (EEG) mostra un’attività lenta e diffusa con rallentamento del ritmo alfa.
Alla TC o alla RMN si può rendere evidente un certo grado di atrofia corticale con ampiamento dei solchi e dilatazione dei ventricoli.
La SPET (tomografia a emissione di fotone singolo) può evidenziare la presenza di ipoperfusione ematica cerebrale mentre la PET (tomografia a emissione di positroni) la riduzione del metabolismo glucidico, in particolare in sede temporo-parieto-occipitale.
Terapia per il morbo di Alzheimer
Non esistono farmaci che permettano di guarire la malattia o di ripristinare le facoltà mentali compromesse. Tuttavia è possibile intervenire nel trattare o contenere le alterazioni affettive e comportamentali e migliorare i disturbi cognitivi.
Gli inibitori selettivi della ricaptazione della serotonina (SSRI) agiscono sull’ansia e sull’agitazione e hanno effetto antidepressivo. Non avendo azione anticolinergica sono da preferire alle benzodiazepine e ai neurolettici.
Gli inibitori dell’acetilcolinesterali (Rivastigmina, Donepezil, Galantamina) sono in grado di migliorare il deficit cognitivo in circa il 35% dei malati. Non è noto con quale meccanismo, ma è stata dimostrata la ridotta produzione di beta-proteina in seguito a stimolazione dei recettori muscarinici dell’acetilcolina.
Nuove terapie per l’Alzheimer?
Sono attualmente oggetto di studio ulteriori terapie, i cui potenziali targets sono:
- meccanismi antinfiammatori che possano aumentare la clearance della proteina A-beta (agendo ad es. sulla funzione della microglia, lo “spazzino” del sistema nervoso centrale);
- la riduzione dello stress ossidativo;
- la riduzione dell’eccito-tossicità mediata dal glutammato;
- la preservazione della funzione neuronale mediante lo studio di meccanismi legati a fattori di crescita, insulina e fattori neurotrofici.
Storia
Il nome della malattia deriva dal nome dello psichiatra e neuropatologo tedesco Alois Alzheimer che a inizio ‘900 descrisse la prima paziente con questa malattia, la signora Auguste D., caratterizzandola da un punto di vista clinico e istopatologico: ella non era in grado di ricordare gli oggetti che le erano stati mostrati pochi minuti prima. Negli anni successivi, il neurologo italiano Gaetano Perusini, ebbe il compito di raccogliere notizie clinico-patologiche su casi analoghi.
N el 1910 A. Alzheimer pubblicò un interessante lavoro a proposito sulla rivista “Histologische und histopathologische Arbeiten über die Grosshirnrinde” (Studi istologici e istopatologici sulla corteccia cerebrale).
el 1910 A. Alzheimer pubblicò un interessante lavoro a proposito sulla rivista “Histologische und histopathologische Arbeiten über die Grosshirnrinde” (Studi istologici e istopatologici sulla corteccia cerebrale).
Nello stesso anno, lo psichiatra tedesco E. Kraepelin parlò per la prima volta di “Malattia di Alzheimer”, inserendola nel suo “Manuale di Psichiatria”.
Per molti anni la malattia di Alzheimer fu considerata una rara demenza presenile. Negli anni ’70 vennero condotti una serie di studi che dimostrarono che la demenza presenile di Alzheimer e la demenza senile avevano il medesimo substrato patologico. Attualmente, perciò, esiste un’unica entità nosologica, la “demenza di Alzheimer” o “demenza primaria degenerativa tipo Alzheimer”: queste denominazione sono utilizzate anche sulla base della sola presentazione clinica, in assenza, cioè, della diagnosi istopatologica.

Dr.ssa Giovanna Russo
Una prevenzione della Malattia di Alzheimer è possibile agendo sui fattori di rischio modificabili: ovvero è necessario adottare un corretto stile di vita, fare regolare attività fisica, alimentarsi in maniera equilibrata, privilegiando frutta e verdura, e non fumare. I fattori di rischio per Alzheimer sono gli stessi delle malattie cardiovascolari!
Certamente impegnarsi in attività che richiedano un impegno cognitivo, quali lettura, cruciverba, sudoku ecc. aiuta a mantenere attivi i circuiti cerebrali e risulta un fattore protettivo. Deve tenere presente che il corpo umano è una macchina dotata di una notevole plasticità e di una incredibile “intelligenza”: se una funzione viene poco o niente utilizzata viene interpretata come inutile e si può avere perdita cellulare.
Se vuole un approfondimento esistono numerosi articoli in letteratura scientifica che affrontano l’argomento. Nell’articolo raggiungibile al seguente link https://www.ncbi.nlm.nih.gov/pubmed/29108888, sono descritti i risultati di uno studio clinico multicentrico controllato randomizzato in doppio cieco, pubblicato nel 2017, in cui è stato studiato l’impatto di fattori modificabili, quali dieta, fattori di rischio cardiovascolari e training cognitivo sulla probabilità di sviluppare un demenza.
A.M88
Salve dottoressa.
Sono a rischio azheimer per motivi familiari, infatti più di una persona nella mia famiglia ne è o è stata affetta.
Vorrei sapere se è possibile prevenire in qualche modo la malattia e come, è vero che possono essere utili delle attività che impegnano il ragionamento come ad esempio scacchi, la lettura o il sudoku?